Білки
1. Поняття про білки
Білки – високомолекулярні полімери, мономерами яких є залишки амінокислот.
Молекулярна маса білків коливаєтся від 10 000 до сотень мільйонів одиниць.
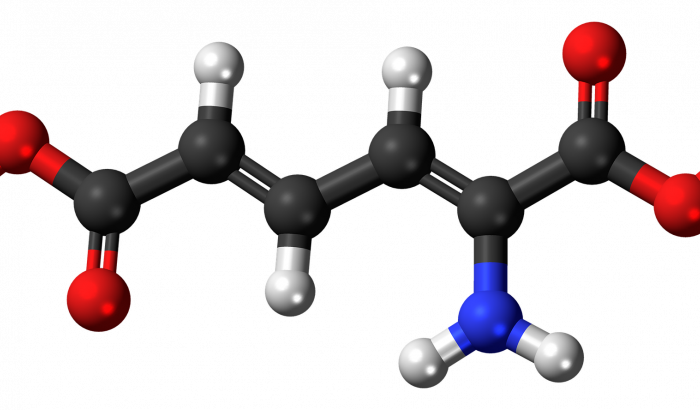
Амінокислота
Білок
2. Будова білкової молекули
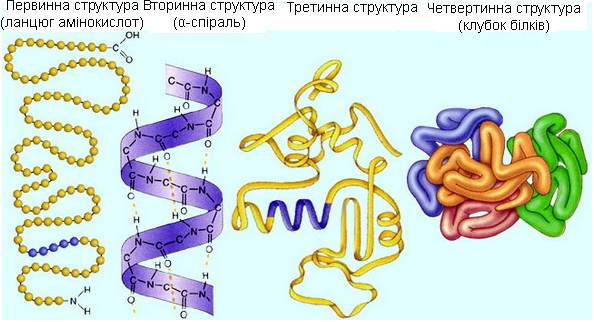
Структура білків
Первинна структура – послідовне лінійне сполучення залишків амінокислот, сполучених пептидними зв’язками
Вторинна структура – спіраль, витки якої сполучені водневими зв’язками
Третина структура – глобула або фібрила, зв’язки водневі, гідрофобні, йонні
Четвертинна структура – поєднання кількох білкових молекул, зустрічається лише в частини білків. Найвідоміший білок з четвертинною будовою молекули — гемоглобін
3. Фізичні властивості білків
Розчинність у воді
Глобулярні білки (альбуміни) розчинні у воді, фібрилярні (колаген, кератин) – нерозчинні.
4. Хімічні властивості білків
Денатурація — руйнування вищих рівнів структурної організації білка – вторинной, третинної, четвертинної.
Денатурація буває оборотна і необоротна.
Оборотна денатурація — від механічної дії, солей, слабких кислот.
Процес відновлення структури білка називається ренатурація.
Необоротна денатурація — вплив високої температури, концентрованих розчинів кислот, лугів, солей важких металів.
Кольорові реакції білків:
Біуретова реакція – синьо-фіолетове забарвлення з купрум (ІІ) гідроксидом.
Ксантопротеїнова реакція – жовте забарвлення під впливом концентрованої нітратної кислоти.
Гідроліз – розпад білка на амінокислоти.
Відбувається під дією кислот та лугів при нагріванні. В організмі — в процесі травлення, під дією ферментів.