Альдегіди
Поняття про альдегіди
Альдегіди — oрганічні речовини, молекули яких складаються з вуглеводневого радикала та карбонільної групи –СОН
Карбонільна група –СОН називається функціональною групою альдегідів
Загальна формула альдегідів — СnH2n+1CHO, або R – CHO
Назва "альдегіди" походить від двох слів: алкоголь і дегідратація, оскільки альдегіди отримують дегідратацією спиртів.
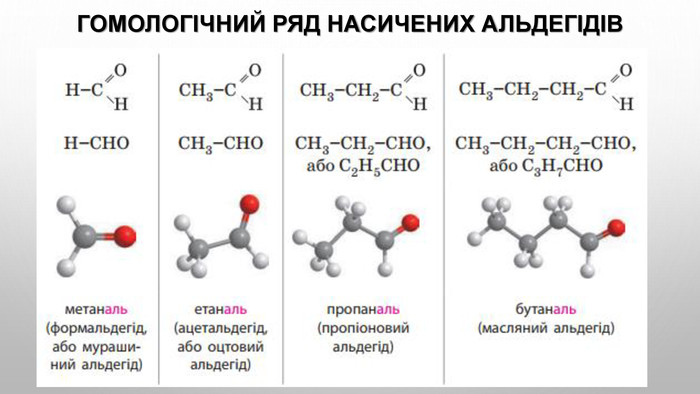
Найпростіші альдегіди
НСОН — метаналь — формальдегід — мурашиний альдегід.
СН3СОН — етаналь — ацетальдегід — оцтовий альдегід.
Альдегіди зустрічаються в природі, вищі альдегіди мають приємний запах.
Одним з перших зразків альдегідних парфумів став культовий аромат Chanel №5 – альдегіди в складі парфумерної формули «подарували» цьому аромату впізнаваний елегантний квітковий запах. Тим не менш, далеко не всі альдегідні з’єднання у складі ароматів володіють яскраво вираженим квітковим запахом: альдегіди можуть пахнути як свіжа зелень, теплий віск, цедра апельсина. Властивості альдегідів універсальні, і саме з цієї причини ці сполуки так цінуються в парфумерії: так, наприклад, альдегід C-11, часто використовується в складі квіткових ароматів володіє яскраво вираженим «металевим запахом», однак у вкрай невеликій кількості, навпаки, додає аромату виняткову свіжість і легкість.

У нерозбавленому ж вигляді альдегіди мають виражений восковий запах.
Як пахнуть найпоширеніші альдегіди:
C-7 - «зелений», трав'янистий аромат
C-8 - апельсиновий запах
C-9 - аромат троянди
C-10 - нагадує по запаху цедру апельсина
C-11 - «природний» альдегід, що видобувається з масла листя коріандру
C-12 - аромат лаванди або фіалки
C-13 - восковий запах з нотками грейпфрута
C-14 - речовина з характерним ароматом персика
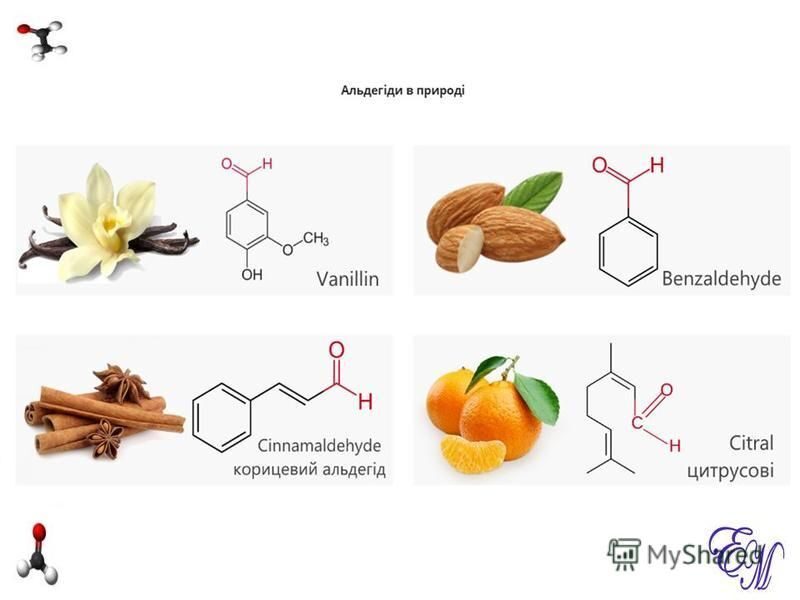
Альдегіди в природі
Фізичні властивості
- метаналь — газ, етаналь — рідина
- без кольору
- з різким неприємним запахом
- токсичні
Водний розчин з масовою часткою формальдегіду 40 % називається формаліном. Є антисептиком. Використовується для дезінфекції та зберігання анатомічних препаратів.
1. Горіння
СН3–СОН + 5О2 → 4СО2 + 4Н2О
2. Відновлення воднем до спиртів
СН3–СОН + Н2 → СН3–СН2–ОН
3. Окиснення до кислот
а) окиснення аргентум оксидом (реакція срібного дзеркала)
СН3–СОН + Ag2O → СН3–СООН + 2Ag
б) окиснення купрум(ІІ) оксидом
СН3–СОН + 2Cu(OH)2 → СН3–СООН + 2CuOH + H2O
CuOH → Cu2O + H2O
Застосування альдегідів
- ароматизатори мила та косметики
- фенолформальдегідні смоли
- у медицині для дезінфекції
- виготовлення анатомічних препаратів
- шанель №5 — перші парфуми з використанням альдегідів
Запам'ятайте. Альдегіди отруйні. Уникайте контакту з альдегідами, не допускайте контакту з ними дітей.